✍
도칠훈
한국전기연구원 전기재료연구본부 차세대전지연구센터 책임연구원
한국과학기술연합대학원대학교(UST) KERI 전기에너지-소재융합 전공 교수
※핵심어: 리튬이차전지, 열화학, 발열, 수명, 캘린더, 싸이클
유기전해질로 고전압화한 리튬이차전지의 新시대
리튬이차전지는 이제 우리 주위에서 흔히 찾을 수 있지만, 1980년대만 해도 리튬이나 소듐을 전지의 전극 재료로 사용하는 건 실현성이 없어서 해결해야 할 난제들이 많았습니다. 리튬금속을 안정적으로 취급할 수 있는 불활성 환경의 영속적 유지와 높은 부식성의 리튬 계면에서도 화학적으로 안정적인 전해질 확보의 어려움 등이었습니다. 당시의 전지는 1차전지와 2차전지를 막론하고 모두 물을 용매로 사용하는 전해질이었습니다. 알려진 바와 같이 Pourbaix diagram1에서 산성이나 염기성에서 물로서 존재할 수 있는 전압은 1.229 V입니다. 유기전해질의 사용으로 고전압화한 리튬이차전지의 상용화는 세계최초로 리튬금속 음극을 적용한 Moli Energy (1990) Ltd.(캐나다)를 시작으로, 탄소재를 음극으로 적용한 Sony(일본, 1991)가 리튬이온전지를 상업화 하면서 그 역사가 이어졌습니다.
1980년대 당시에는 metal hydride 화합물(금속수소화물)에 대한 개념이 보편화 되었고, 수소기체를 금속수소화물로 고형화하고 이를 고밀도의 가역적 과정으로 전환하는 많은 연구가 진행되었습니다. 주요 응용처는 수소기체의 고밀도 저장과 이차전지로의 응용이었습니다. 금속수소화물 중의 수소의 산화상태는 -1에 가까워서 통상 알고 있는 물을 구성하는 수소의 산화수 +1과는 상당히 다른 화학 분야가 됩니다. 1990년대에는 금속수소화물의 비약적인 발전으로 니켈산화물-금속수소화물(니켈-수소) 이차전지가 상용화되었습니다. 기존의 이차전지 전문 업체들은 상당 기간 동안 니켈수소전지의 시대가 될 것으로 전망하며 생산력을 확장하던 시기였습니다. 리튬이차전지(Moli Energy)의 불안정성이 확인되면서 니켈수소전지의 장기전망 추세는 타당한 것으로 여겨졌습니다.
불안정성의 원인인 리튬금속 음극을 탄소(흑연)로 대체하여 불안정성 문제를 극복한 리튬이차전지는 모바일 정보통신의 비약적인 발전을 이끌어왔고, 현재 세계인이 일상으로 사용하고 있습니다. 리튬이차전지의 우수성은 1990년대부터 현재까지 약 30년의 사용으로 검증된 것이라고 볼 수 있습니다.
물론 전지는 화학반응을 하는 일개의 장치로서 물리현상을 사용하는 장치에 비교하여 수명이 현저히 낮습니다. 이러한 이유로 전지 사용자는 전지 수명의 한계를 겪으면서 늘 ‘전지는 문제가 많다’는 결론에 도달합니다. 전지 개발자로서는 늘 가까이서 들려오는 반농담의 불평 섞인 얘기를 듣게 됩니다.
리튬이차전지는 초기와 비교하여 비약적으로 고성능화 되어, 내재(잠재)하고 있는 전기화학 에너지 또한 지속적으로 증가하였습니다. 지난 30년간의 발전과 검증으로 응용분야가 급격히 팽창하고 있고, 단위전지의 크기도 증가할 뿐만 아니라 직렬과 병렬 집합전지2의 규모도 급증 추세입니다.
전자회로적 제어로 전지의 내재에너지에 의한 불안정성을 제어함으로써 문제를 억지하고 있습니다. 하지만 전자회로적 안정화에도 불구하고 전지와 제어장치의 결함으로 전지 시스템이 위험에 노출되기도 합니다.
요약하면 소형전지의 성능과 안정성은 충분히 검증되었다고 할 수 있으나, 응용분야의 다각화로 전지의 대형화, 직·병렬화가 요구됨에 따라 전지의 수명과 안정성에 대한 이슈는 여전히 제기되고 있습니다.
리튬이차전지의 전기-열-화학
먼저, 안정성에 대하여 살펴보고자 합니다. 전지의 안정성은 외형의 변형이 없는 폐쇄계의 범주에서 온도의 증감으로 나타낼 수 있습니다. 전지의 정상 충·방전이나 단락 저항 방전에서 온도의 변화는 줄 발열(Joule heating)과 전지재료의 internal energy의 변화를 나타내는 앤트로피 기여분의 변화에 따른 발열(Entropical heating)로 나타납니다. 많은 연구자들이 시간의 변화에 대하여 열화학 변화를 해석해 왔는데, 온도변화를 충전상태(SOC; state of charge)의 변화에 대하여 기술하여 가역 반응을 조금 더 쉽게 표현하고자 하였습니다.
그림 1은 정전류 충·방전과 외부단락을 모의하는 정외부저항(constant external resistance) 방전에 대하여 미분충전상태의 함수로 표현한 관계입니다. 충전 상태에 따른 온도 변화 관계와 함께 시간에 대해서도 표현할 수 있습니다.
정전류 충방전 과정에서 앤트로피의 변화와 충전상태와 온도에 따른 전지내부저항의 변화로부터 전지의 고유특성인 전지용량, 전지중량, 전지비열을 적용하여 시험해 보지 않은 새로운 조건의 초기 충전상태, 초기 온도와 전류(C율)의 미지 조건에 대한 충·방전 과정 중 전지의 충전상태별 온도, 내부저항, 앤트로피 등 특성을 알 수 있습니다.
또한, 정외부저항 방전은 전지의 전압과 전류가 동시에 변동하는 전류 흐름 조건입니다. 정외부저항 방전의 관계 해석은 정전류 충·방전과 유사한 관계로 주어질 수 있는데, 개회로전압과 전지-부하의 결선 저항과 외부 부하의 저항의 추가 인자를 적용하여 해석할 수 있습니다.
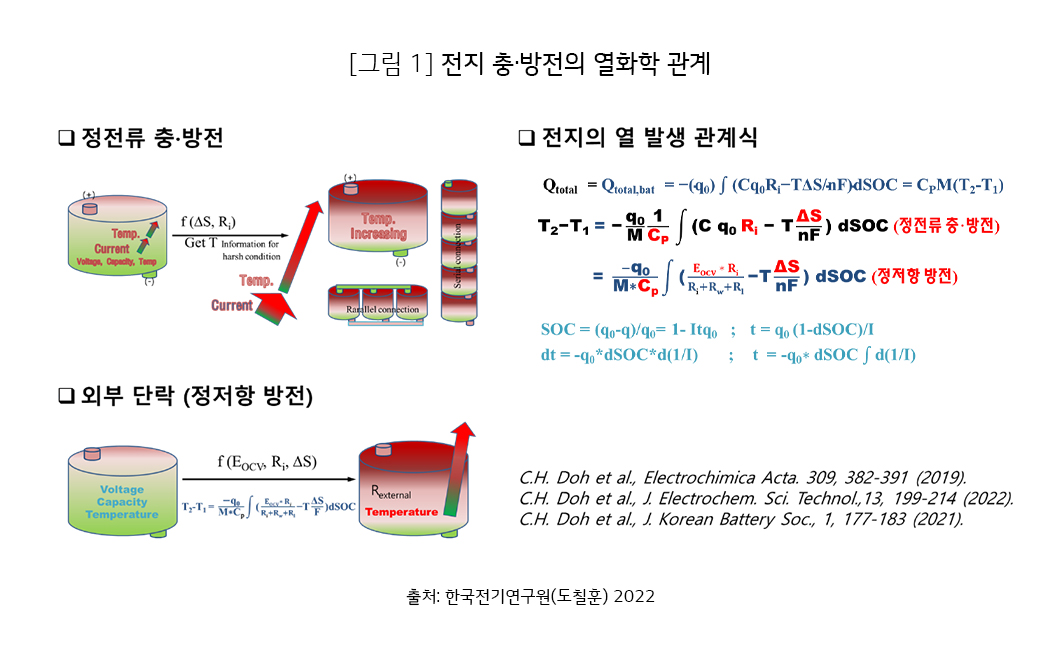
[ T1,T2,T: 초기 온도와 최종온도와 온도 (K); q0: 전지용량 (Ah, coulomb); M: 전지중량; Cp: 비열; C: 전지 충·방전율(C-rate); Ri:전지 내부저항(SOC와 온도의 함수 관계); EOCV: 개회로전압; Ri: 전지의 내부저항; Rw: 전지와 부하의 결선 저항; Rl: 외부 부하의 정저항; n: 충·방전전기량의 몰수 (mole); F: Faraday 상수 (96,485 coulomb/mol); SOC: state of charge of cell. ]
그림 2는 계산식의 한 응용 예로서 주어진 초기 정전류 충·방전 초기 조건에 대하여 최종 온도를 구한 결과입니다. 초기 온도 18℃, 35℃, 60℃에 대하여 충전이나 방전의 C율을 20C까지 변화하면서 구하였습니다. 충전 과정을 보면 C율의 증가에 따라서 전지 온도가 증가하여 10C율에서 117℃ 정도로 승온하는 결과를 보여줍니다. 초기 온도가 달라도 같은 결과임을 보여줍니다. 방전 과정도 충전과 같은 경향이고 승온 속도는 충전보다 빠릅니다. 10C율 방전에서 187℃ 정도로 승온하는 결과를 보여줍니다.
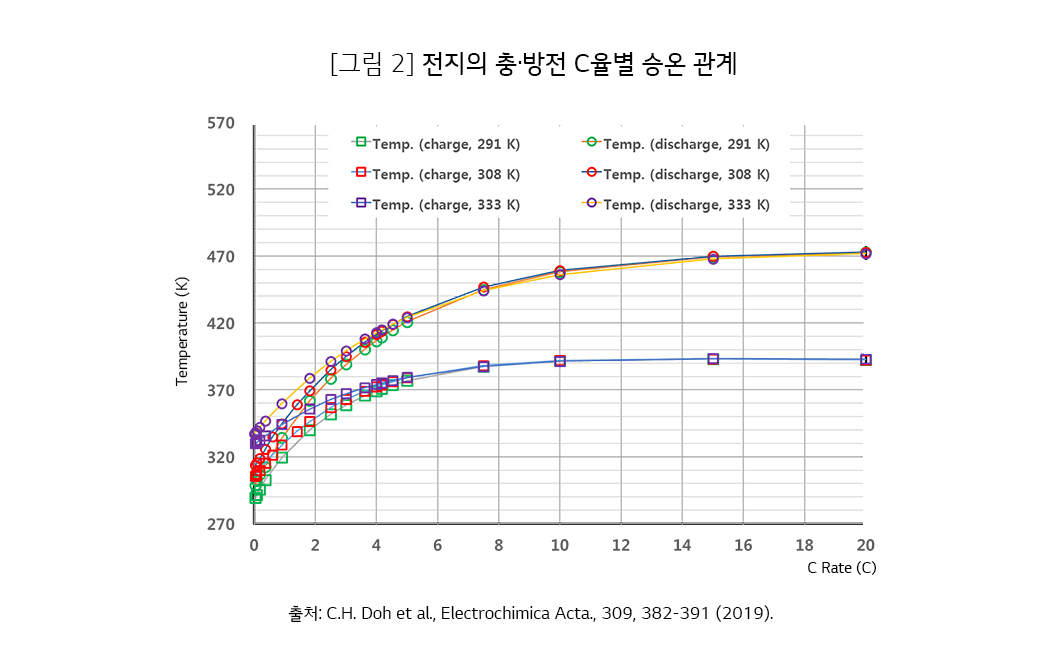
외부단락에서 외부저항에 따른 최종 온도를 초기온도와 초기충전상태에 대하여 계산한 결과를 그림 3에 나타냈습니다. 외부저항 11 mΩ의 경우에는 80℃ 이하 수준이고, 외부저항 2 mΩ 이하의 경우에는 150℃ 이상까지 승온할 수 있다는 것을 나타냅니다. 보다 자세한 사항은 그림 1에 나타낸 참고 문헌에서 보실 수 있습니다.
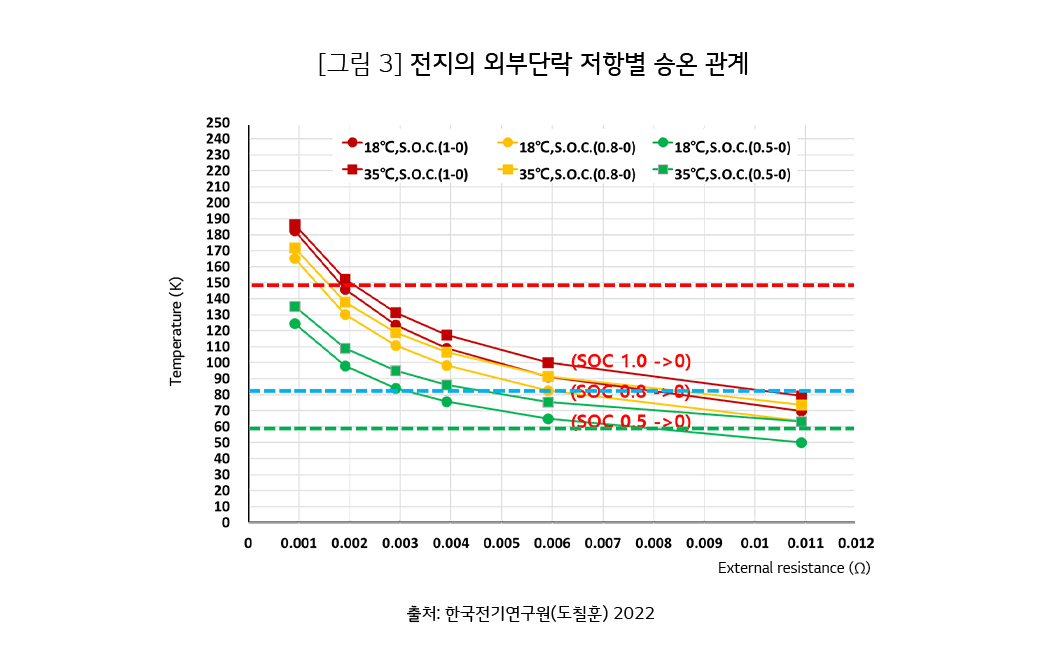
전지 성능을 보다 정확하고 용이하게 계산하기 위한 한 방안으로서 본 설명에서의 미분충전상태 기반의 계산을 제안하고 응용 예를 소개하였습니다.
리튬이차전지의 수명
전지의 수명에 대한 많은 보고가 있으며, 대부분 싸이클 수명을 논하여 왔습니다. 싸이클 수명은 충·방전심도(DOD, depth of discharge), 평균 충전상태(SOC, state of charge), 온도, 충방전율의 변화에 따라서 매우 크게 다른 결과로 나타납니다. 관심 깊게 볼 수 있는 한 부류의 방법이 stress factor model(SFM)3입니다. SFM은 싸이클 수와 시간의 복합 관계로 전지의 퇴화를 구하는 관계식과 인자의 함수관계를 도출하여 수명을 구합니다. 싸이클 수와 시간의 복합 관계를 적용하고 무차원화하여 퇴화(fade)를 구하는 방법은 효과적입니다. SFM 관계식의 결과를 실험과 비교해 보면 오차가 나타나기도 합니다.
SFM의 오차 원인을 해소하기 위한 한 방법으로 싸이클 수와 시간의 이중 변수의 표현을 시간의 단일 변수로 표현하고자 검토하였는데, 주어진 충·방전 조건에 대해서 싸이클 수를 시간의 관계로 표현할 수 있었습니다. 따라서 전지의 수명에 영향을 끼치는 인자는 요약하여 온도, 평균 SOC, DOD, C율, 시간이라고 볼 수 있습니다.
SFM에서 전지 수명의 전체 영역을 계산하기 위해서는 비선형적 부분을 포함하여야 하지만, 실질적으로 사용하기에 유효한 잔존 용량인 60~70% 수준까지는 직선적인 관계로 볼 수 있습니다. 이러한 관계를 종합하여 아래의 수식으로 나타낼 수 있습니다.
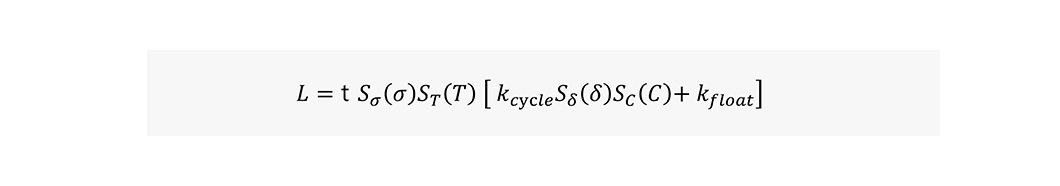
[ L: capacity fade ratio; t: time; ??(?); SOC 스트레스 펙터; ??(?): 온도 스트레스 펙터; ??(?): DOD 스트레스 펙터; ??(?): C율 스트레스 펙터; ??yc??: 싸이클 스트레스 펙터 모델 계수; ??????: 플로팅 스트레스 펙터 모델 계수. ]
??????은 시간에 흐름에 따른 기준 조건의 열화 속도 상수가 되고, ?cycle은 싸이클 동안에 경과하는 시간에 의한 열화를 제외한 기준 조건의 열화 속도 상수로 구할 수 있습니다. ?cycle은 2개 이상의 다른 조건으로 구한 복합 열화 속도 상수(??alendar)로 부터 분리 할 수 있습니다.

전지용량 5 Ah/cell에 대한 기준조건으로 온도 40℃, SOCave 50%, DOD 90%, C율 C/3, 휴식시간 0시간에 대한 ??alendar는 7.234E-04 day-1이고, 휴식시간 10일로 한 ??alendar는 5.634E-04 day-1으로 구하였습니다.
Floating SOC를 기준으로 구한 ?cycle은 4.802E-04 day-1이고 kfloat 은 2.433E-04 day-1이었으며, floating time을 기준으로 구한 ?cycle은 1.032055E-03 day-1이고 kfloat은 2.345725E-04 day-1로 각각 구할 수 있었습니다.
싸이클 수(Cn)는 전체 소요시간에 대한 1회 평균 싸이클 소요시간의 관계이고, 평균 싸이클 소요시간은 선형적인 용량 퇴화의 조건에서 다음 식의 관계가 됩니다. 여기서 L은 capacity fade ratio의 수명 한계 조건입니다.

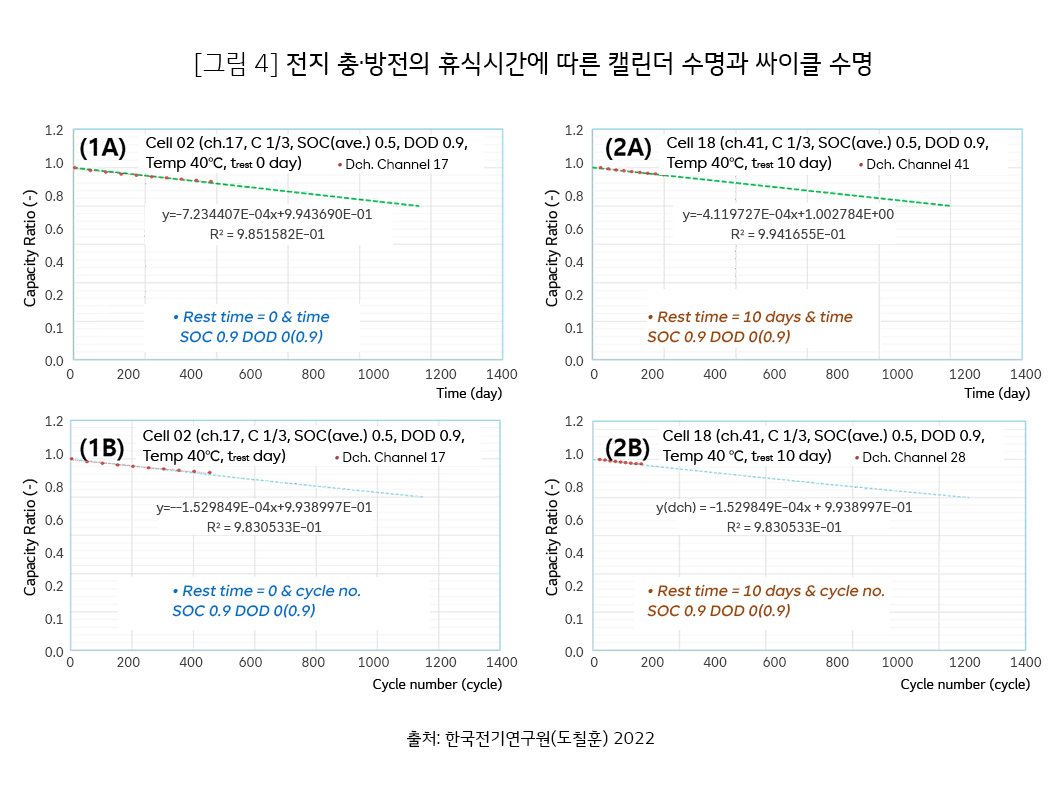
Floating time을 기준으로 구한 ??yc??과 ?float을 적용하여 구한 결과를 실험 결과와 비교하여 전지 잔존 용량 80%까지의 calendar 수명과 싸이클 수명을 그림 4에 나타내었습니다. 충방전 사이의 floating 시간을 주지 않은 경우와 10일을 준 경우에 대한 실험과 계산 결과를 (1)과 (2)로 나타내었습니다. 휴식시간을 주지 않은 (1A)에서는 250일 정도의 수명을 나타내었고, 싸이클링을 적게한 (2A)에서는 500일 정도의 수명을 나타내었습니다. 또한, x-축을 싸이클 수로 나타낸 (1B)와 (2B)의 비교에서는 휴식시간이 없을 때 싸이클 수명이 약 1150회에 달하고 10일휴식일 때 220회 정도로 나타났습니다.
이외에 온도, DOD, 평균 SOC, 휴식시간, C율의 변화에 대한 연계 분석을 진행하고 있으며 추후에 종합하여 보고하고자 합니다.
상기에서 살펴본 리튬이차전지의 수명과 안전성(열화학) 연구는 최첨단 전지 산업의 밑거름 기술을 개발하는 것이기도 하며, 전지의 대형화 집합화에 대한 근간 기술을 제공하는 분야이므로 실험과 물리/화학 기반의 모델링을 연계하는 집중적인 연구가 필요한 분야이기도 합니다.
끝으로 고에너지밀도의 에너지저장장치인 리튬이차전지의 수명·안전성(열화학)과 전고체화의 신기술을 궁구하는 과학기술인 모든 분들께 인사를 전합니다.
1 E-pH Diagram of Water, https://corrosion-doctors.org/Corrosion-Thermodynamics/ Potential-pH-diagram-water.htm, Sep. 2022.; Pourbaix diagram, https://en.wikipedia.org/wiki/Pourbaix_diagram, Sep. 2022.
2 유용원, 군용 전지 실태와 시장 전망, Battery Inside, LG Energy Solution, April. 26. 2022.
3 Bolun Xu, Alexandre Oudalov, Andreas Ulbig, Göran Andersson, Daniel S. Kirschen, Modeling of Lithium-Ion Battery Degradation for Cell Life Assessment, IEEE TRANSACTIONS ON SMART GRID, 9(2), (2018), 1131-1140.
※ 이 칼럼은 해당 필진의 소견이며 LG에너지솔루션의 입장이나 전략을 담고 있지 않습니다.





