스마트폰을 켜고, 전기차를 움직이는 그 순간, 배터리 안에서는 보이지 않는 입자들이 끊임없이 움직이고 있습니다. 전자와 리튬이온이 만들어내는 흐름은 어떻게 전류가 될까요? 배터리 내부에서 일어나는 과정을 단계별로 따라가 봅니다.

쉽게 말해 배터리는 내부의 산화-환원 반응으로 발생한 전자의 흐름을 전기 에너지로 전환하는 장치입니다. 이를 이해하려면 먼저 배터리의 구성요소를 이해해야 합니다.
STEP 0 배터리의 본질
리튬이온배터리는 크게 4가지 핵심 소재로 구성됩니다.
- 양극(Cathode): 방전 시 리튬이온을 받아들이는 전극
- 음극(Anode): 방전 시 리튬이온을 방출하는 전극
- 전해질(Electrolyte): 리튬이온이 두 전극 사이를 이동할 수 있도록 돕는 매개체
- 분리막(Separator): 양극과 음극이 직접 닿지 않도록 막아주는 절연층
배터리는 전기를 그대로 저장하는 장치가 아닙니다. 배터리는 내부에 저장된 화학 에너지를 전기 에너지로 변환하여 작동하죠.
배터리에서 일어나는 화학 반응은 크게 산화(Oxidation)와 환원(Reduction)입니다.
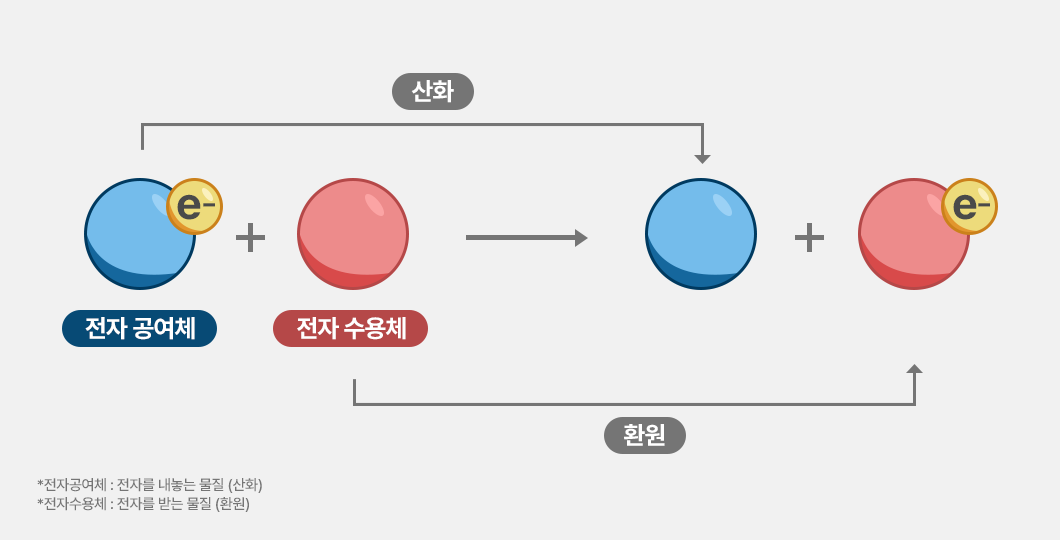
- 산화: 전자를 잃는 것
- 환원: 전자를 얻는 것
원자는 핵과 그 주위를 도는 전자로 이루어져 있습니다. 전자가 원자 밖으로 나와 이동하면 전류가 형성됩니다. 일반적으로 배터리를 사용할 때(방전 시), 양극에서는 환원 반응이 일어나고 음극에서는 산화 반응이 일어납니다. 그리고 이 산화와 환원 반응은 항상 동시에 발생합니다. 한쪽에서 전자를 내놓으면, 다른 한쪽이 반드시 그 전자를 받아야 하기 때문입니다. 이 두 반응을 합쳐 산화-환원 반응(Redox)이라고 합니다.
STEP 1 전류가 흐르기 위한 조건 ‘전위차’
그렇다면 전자는 어떤 힘에 의해 이동할 수 있을까요? 이는 양극과 음극 두 전극 사이에 전위차(Potential Difference)가 존재하기 때문입니다.
전위는 전기장 내에서 단위 전하가 가지는 전기적 위치 에너지를 의미하며, 단위는 볼트(V)를 사용합니다. 일반적으로 전하는 전위가 높은 곳에서 낮은 곳으로 이동하려는 경향이 있으며, 이 차이가 클수록 이동하려는 힘이 커집니다. 이처럼 두 지점 사이에 전위차가 형성되면, 그 차이에 의해 전하가 이동하고 전류가 흐르게 됩니다. 우리가 흔히 말하는 전압(V)은 바로 이 전위차를 의미합니다.
이 전위를 비교하기 위해 수소/수소이온 반응을 기준(0V)으로 설정한 값이 표준환원전위입니다. 표준환원전위는 표준 상태에서 수소보다 환원이 잘되면 양(+)의 값을 가지며, 값이 음(-)일수록 전자를 쉽게 내놓아 산화되기 쉬운 물질입니다. 예를 들어 리튬의 표준환원전위는 -3.04V로, 매우 쉽게 산화되는 금속입니다.
STEP 2 음극에서 일어나는 일: 산화 반응
이처럼 전위차가 존재하더라도, 전자가 이동할 수 있는 경로가 없다면 전류는 흐르지 않습니다. 하지만 배터리가 외부 회로와 연결되는 순간, 전자는 이동을 시작하고 전기화학 반응이 진행됩니다.
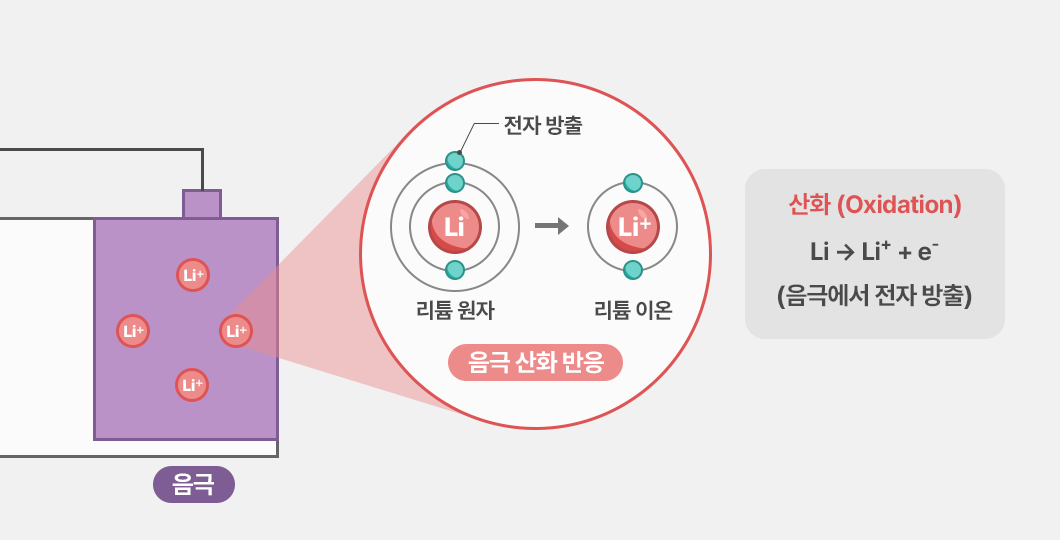
이때 음극에서는 리튬이 산화되며 다음과 같은 반응이 일어납니다.
- Li → Li⁺ + e⁻
음극에 저장되어 있던 리튬은 전자를 잃고 리튬이온(Li⁺)과 전자(e⁻)로 전환됩니다. 즉, 리튬이온과 전자가 분리되는 지점이자 전류가 시작되는 출발점이죠.
STEP 3 리튬이온과 전자가 양극으로 이동하는 과정
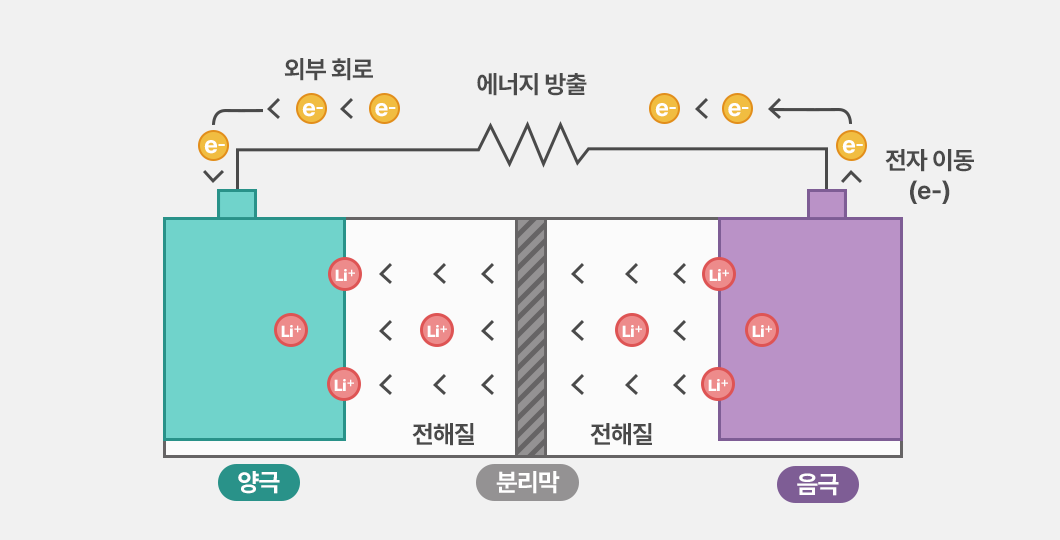
음극에서 분리된 리튬이온과 전자가 양극을 향해 이동하면서, 배터리 내부와 외부에서는 하나의 연결된 흐름이 형성됩니다.
이때 전자는 외부 회로를 따라 이동하며 전류를 만들고, 이 전류가 기기에 전달되면서 실제로 에너지가 사용됩니다. 즉, 전자의 이동은 단순한 이동이 아니라 전기 에너지가 전달되는 과정입니다.
한편, 리튬이온은 전해질을 통해 이동하면서 전극 사이의 전기적 균형을 유지하는 역할을 합니다. 전자와 리튬이온이 동시에 이동해야만 전체 반응이 끊기지 않고 지속될 수 있습니다.
이 과정에서 분리막은 전자의 내부 이동을 차단해 전류가 반드시 외부 회로를 통해 흐르도록 만듭니다. 만약 전자가 배터리 내부로 직접 이동하면 단락(Short Circuit)이 발생하게 되죠.
STEP 4 양극에서 일어나는 일: 환원 반응
외부 회로를 따라 이동한 전자와 전해질을 통해 이동한 리튬이온은 양극에서 다시 만납니다. 리튬이온은 양극 구조 안으로 삽입되고, 동시에 전자가 유입되죠. 이 과정에서 전이금속이 전자를 받아들이는 환원 반응이 일어납니다.
예를 들어 LFP 양극재에서는 철(Fe)이 전자를 받아 환원되고, NCM, NCA 계열에서는 니켈(Ni)이 이를 주로 담당합니다.
이처럼 리튬이온과 전자의 삽입은 하나의 연속된 반응으로 진행되며, 전자는 반응 과정에서 전달 역할을 하는 매개체로 작용합니다. 이러한 반응이 지속되는 동안 전자는 외부 회로를 따라 계속 흐르고, 전류가 유지됩니다.
STEP 5 충전: 반응을 거꾸로 되돌리기
전자가 흐르고 양극이 이를 지속적으로 받아들이는 전체 과정을 방전(Discharge)이라고 합니다. 방전은 에너지가 낮아지는 방향으로 진행되기 때문에 자발적으로 일어납니다.
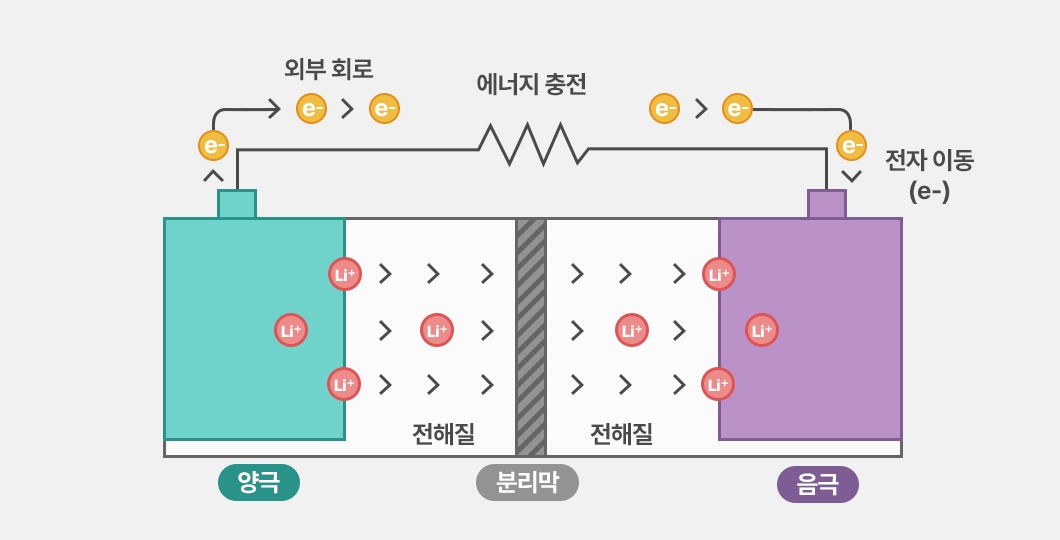
반면 충전(Charge)은 외부 에너지를 이용해 방전 과정을 역방향으로 되돌리는 과정입니다. 충전 시에는 외부에서 인가된 전압에 의해 형성된 전기장이 반응을 역방향으로 진행시키며, 리튬이온은 다시 음극으로 이동합니다. 이때 전자는 외부 전원을 통해 음극으로 공급되고, 리튬이온은 전해질을 통해 이동하여 음극에 다시 저장됩니다.
즉, 충전은 외부 전압에 의해 전기화학 반응이 비자발적으로 진행되는 과정입니다.
핵심 Q&A
Q. 배터리는 전기를 저장하는 장치인가요?
배터리는 전기를 그대로 저장하는 장치가 아니라, 전기 에너지를 화학 에너지 형태로 변환해 저장한 뒤 필요할 때 다시 전기 에너지로 바꾸는 전기화학 시스템입니다.
Q. 배터리에서 전류는 어떻게 만들어지나요?
음극에서는 산화 반응을 통해 전자가 방출되고, 이 전자가 외부 회로를 따라 이동하면서 전류가 형성됩니다. 동시에 리튬이온은 전해질을 통해 양극으로 이동하고, 양극에서는 환원 반응이 일어나면서 이 흐름이 이어집니다.
Q. 리튬이온과 전자는 왜 서로 다른 경로로 이동하나요?
리튬이온은 전해질을 통해 이동하고, 전자는 내부를 통과하지 못하도록 분리막이 차단하기 때문에 외부 회로를 따라 이동합니다. 이 구조 덕분에 전자는 반드시 외부로 흐르게 되고, 그 결과 전류가 발생합니다.
Q. 충전할 때는 배터리 내부에서 어떤 일이 일어나나요?
충전 시에는 외부 전압이 가해지면서 방전 과정이 반대로 진행됩니다. 전자는 외부 전원을 통해 음극으로 이동하고, 리튬이온도 전해질을 통해 음극으로 이동하면서 다시 저장됩니다.
배터리 작동 원리는 전자가 이동하고, 리튬이온이 전해질을 통해 이동하며, 전극에서 이를 받아들이는 반응이 이어지는 하나의 흐름으로 설명할 수 있습니다. 이 과정이 지속되는 동안 전류가 형성되고, 이를 통해 기기가 작동하게 됩니다.
이처럼 배터리는 전기를 저장하는 장치가 아니라, 화학 반응을 통해 전기를 만들어내는 시스템입니다. 결국 배터리를 이해하는 핵심은 이 흐름을 정확히 이해하는 데 있습니다. 이처럼 배터리를 이해할 때는 전자와 리튬이온의 이동, 그리고 전극에서 일어나는 반응이 어떻게 이어지는지 그 흐름에 주목해 보세요.





